NCERT Class 10 Science Chapter 5 तत्वों के आवर्त वर्गीकरण
NCERT Solutions for Class 10 Science Chapter 5 तत्वों के आवर्त वर्गीकरण
एनसीईआरटी समाधान अंतर्पाठीय प्रश्न
पृष्ठ संख्या: 81
प्रश्न 1
क्या न्यूलैंड्स के अष्टक के स्तंभों में डोबेरिनर के त्रिक भी मौजूद थे? तुलना करके पता लगाएँ।
उत्तर:
हाँ, न्यूलैंड्स के अष्टक के स्तंभों में डोबेरिनर के त्रिक भी मौजूद थे।
उदाहरण के लिए, Li, Na, K.
यदि हम लिथियम (Li) को पहला तत्व मानते हैं, तो सोडियम (Na) आठवाँ तत्व है। यदि हम सोडियम को पहला तत्व मानते हैं, तो पोटैशियम आठवाँ तत्व है।
प्रश्न 2:
डोबेराइनर के वर्गीकरण की सीमाएँ क्या थीं?
उत्तर:
यह उस समय ज्ञात सभी तत्वों को समान रासायनिक गुणों वाले तत्वों के त्रिक के रूप में व्यवस्थित करने में विफल रहा। डोबेराइनर उस समय ज्ञात तत्वों में से केवल तीन त्रिक की पहचान कर सके।
प्रश्न 3
न्यूलैंड्स के अष्टक नियम की सीमाएँ क्या थीं?
उत्तर:
(i) न्यूलैंड्स का अष्टक नियम केवल कैल्शियम तक के तत्वों के वर्गीकरण पर लागू था। कैल्शियम के बाद हर आठवें तत्व में पहले तत्व के समान गुण नहीं थे।
(ii) न्यूलैंड्स ने मान लिया था कि प्रकृति में केवल 56 तत्व मौजूद हैं और भविष्य में और तत्वों की खोज नहीं की जाएगी। लेकिन बाद में, कई नए तत्वों की खोज की गई जिनके गुण न्यूलैंड्स के अष्टक नियम में फिट नहीं होते थे।
(iii) तत्वों को अपनी तालिका में फिट करने के लिए, न्यूलैंड्स ने दो तत्वों को एक साथ एक स्लॉट में रखा और वह भी बहुत अलग गुणों वाले असमान तत्वों के कॉलम में। उदाहरण के लिए, दो तत्व कोबाल्ट (Co) और निकल (Ni) को सिर्फ एक स्लॉट में एक साथ रखा गया था
और वह भी फ्लोरीन, क्लोरीन और ब्रोमीन जैसे तत्वों के कॉलम में,
पृष्ठ संख्या: 85
प्रश्न 1
निम्नलिखित तत्वों के ऑक्साइडों के सूत्रों की भविष्यवाणी करने के लिए मेंडेलीव की आवर्त सारणी का उपयोग करें: K, C, Al, Si, Ba
उत्तर:
K 2 O, CO 2 , Al 2 O 3 , SiO 2 , BaO.
प्रश्न 2
गैलियम के अलावा, अब तक कौन से अन्य तत्वों की खोज की गई है जिन्हें मेंडेलीव ने अपनी आवर्त सारणी में छोड़ दिया था? (कोई दो)
उत्तर:
स्कैंडियम और जर्मेनियम।
प्रश्न 3
मेंडेलीव ने अपनी आवर्त सारणी बनाने के लिए किन मानदंडों का इस्तेमाल किया?
उत्तर:
मेंडेलीव ने तत्वों के परमाणु द्रव्यमान और उनके भौतिक एवं रासायनिक गुणों के बीच संबंध का इस्तेमाल किया। उन्होंने भौतिक गुणों में समानता, तत्वों के हाइड्राइड और ऑक्साइड के निर्माण में समानता का इस्तेमाल किया।
प्रश्न 4
आपके विचार से उत्कृष्ट गैसों को एक अलग समूह में क्यों रखा गया है?
उत्तर:
उत्कृष्ट गैसें रासायनिक रूप से निष्क्रिय होती हैं और वायुमंडल में अत्यंत कम सांद्रता में मौजूद होती हैं। इसलिए, उनके समान निष्क्रिय व्यवहार और समान इलेक्ट्रॉनिक विन्यास के कारण, उन्हें एक अलग समूह में रखा जाना उचित है।
पृष्ठ संख्या: 90
प्रश्न 1
आधुनिक आवर्त सारणी मेंडेलीव की आवर्त सारणी की विभिन्न विसंगतियों को कैसे दूर कर सकती है?
उत्तर:
(i) आधुनिक आवर्त सारणी परमाणु क्रमांक पर आधारित है, जबकि मेंडेलीव की आवर्त सारणी परमाणु द्रव्यमान पर आधारित थी।
(ii) किसी तत्व के समस्थानिकों में प्रोटॉन (या परमाणु क्रमांक) की संख्या समान होती है। इसलिए उन्हें आधुनिक आवर्त सारणी में समान स्थान दिया गया है।
(iii) कोबाल्ट और निकल को क्रमशः 9वें और 10वें स्थान पर रखा गया है।
(iv) हाइड्रोजन को विशेष स्थान दिया गया है, अर्थात इसे पहले समूह में क्षार धातुओं में सबसे ऊपर रखा गया है।
प्रश्न 2
दो ऐसे तत्वों के नाम बताइए जिनसे आप मैग्नीशियम के समान रासायनिक अभिक्रियाएँ प्रदर्शित करने की अपेक्षा करते हैं। आपके चयन का आधार क्या है?
उत्तर:
बेरिलियम (Be) और कैल्शियम (Ca)।
Be (परमाणु क्रमांक 4) और Ca (परमाणु क्रमांक 20) दोनों का इलेक्ट्रॉनिक विन्यास समान है, अर्थात सबसे बाहरी कोश में दो इलेक्ट्रॉन होते हैं।
Be 2,2
Ca 2, 8, 8, 2
Be और Ca दोनों ऑक्सीजन के साथ अभिक्रिया करके क्षारीय ऑक्साइड, BeO और MgO देते हैं।
प्रश्न 3
नाम :
(a) तीन तत्व जिनके सबसे बाहरी कोश में एक इलेक्ट्रॉन होता है।
(b) दो तत्व जिनके सबसे बाहरी कोश में दो इलेक्ट्रॉन होते हैं।
(c) तीन तत्व जिनके सबसे बाहरी कोश भरे हुए हैं।
उत्तर :
(a) लिथियम : परमाणु संख्या - 3(2, 1); सोडियम : परमाणु संख्या - 11(2, 8, 1); पोटेशियम : परमाणु संख्या - 19(2, 8, 8, 1)।
(b) बेरिलियम : परमाणु संख्या - 4(2, 2); कैल्शियम : परमाणु संख्या - 20(2, 8, 8, 2)
(c) हीलियम : परमाणु संख्या - 2(2); निऑन : परमाणु संख्या - 10(2, 8); आर्गन : परमाणु संख्या - 18(2, 8, 8)।
प्रश्न 4
(a) लिथियम, सोडियम, पोटेशियम सभी धातुएँ हैं जो हाइड्रोजन गैस मुक्त करने के लिए पानी के साथ प्रतिक्रिया करती हैं। क्या इन तत्वों के परमाणुओं में कोई समानता है?
(b) हीलियम एक अक्रियाशील गैस है और निऑन अत्यंत कम प्रतिक्रियाशीलता वाली गैस है। यदि कुछ है, तो उनके परमाणुओं में क्या समानता है?
उत्तर:
(a) लिथियम, सोडियम और पोटेशियम सभी एक ही समूह से संबंधित हैं। लिथियम, सोडियम और पोटेशियम के परमाणुओं के सबसे बाहरी कोश में केवल एक इलेक्ट्रॉन होता है और ये सभी धातु हैं। ये सभी पानी के साथ प्रतिक्रिया करके क्षार बनाते हैं।
(b) हीलियम और निऑन के परमाणुओं के सबसे बाहरी कोश पूरी तरह से भरे हुए हैं। हीलियम का पहला कोश पूरी तरह से भरा हुआ है, जबकि निऑन का पहला और दूसरा कोश (K और L) पूरी तरह से भरा हुआ है।
प्रश्न 5
आधुनिक आवर्त सारणी में, पहले दस तत्वों में कौन-सी धातुएँ शामिल हैं?
उत्तर:
आधुनिक आवर्त सारणी में पहले दस तत्व हाइड्रोजन, हीलियम, लिथियम, बेरिलियम, बोरॉन, कार्बन, नाइट्रोजन, ऑक्सीजन, फ्लोरीन और निऑन हैं। इनमें से लिथियम, बेरिलियम और बोरॉन धातु हैं, क्योंकि इनके सबसे बाहरी कोश में क्रमशः 1, 2 और 3 इलेक्ट्रॉन होते हैं।
प्रश्न 6
आवर्त सारणी में उनके स्थान को देखते हुए, आप निम्नलिखित में से किस तत्व में अधिकतम धात्विक विशेषताएँ होने की अपेक्षा करेंगे?
Ga, Ge, As, Se, Be
उत्तर:
बेरिलियम (Be)। आवर्त सारणी में, बाईं ओर स्थित तत्व अधिकतम धात्विक विशेषताएँ प्रदर्शित करते हैं। चूँकि बेरिलियम अन्य तत्वों की तुलना में सबसे बाईं ओर स्थित है, इसलिए यह अधिकतम धात्विक विशेषताएँ प्रदर्शित करता है।
कक्षा 10 विज्ञान अध्याय 5 पाठ्यपुस्तक अध्याय के अंतिम प्रश्न के लिए एनसीईआरटी समाधान
प्रश्न 1
आवर्त सारणी के आवर्तों में बाएँ से दाएँ जाने पर प्रवृत्तियों के बारे में निम्नलिखित में से कौन सा कथन सही नहीं है?
(a) तत्वों की प्रकृति कम धात्विक हो जाती है।
(b) संयोजकता इलेक्ट्रॉनों की संख्या बढ़ जाती है।
(c) परमाणु अपने इलेक्ट्रॉनों को अधिक आसानी से खो देते हैं।
(d) ऑक्साइड अधिक अम्लीय हो जाते हैं।
उत्तर:
(c) परमाणु अपने इलेक्ट्रॉनों को अधिक आसानी से खो देते हैं।
प्रश्न 2 तत्व X, XCl2
सूत्र वाला एक क्लोराइड बनाता है , जो उच्च गलनांक वाला ठोस है। X, आवर्त सारणी के किस समूह में सबसे अधिक सम्भवतः है? (a) Na (b) Mg (c) Al (d) Si उत्तर: (b) Mg
प्रश्न 3
किस तत्व में
(a) दो कोश होते हैं, जिनमें से दोनों पूरी तरह से इलेक्ट्रॉनों से भरे होते हैं ?
(b) इलेक्ट्रॉनिक विन्यास 2, 8, 2 ?
(c) कुल तीन कोश होते हैं, जिसके संयोजकता कोश में चार इलेक्ट्रॉन होते हैं ?
(d) कुल दो कोश होते हैं, जिसके संयोजकता कोश में तीन इलेक्ट्रॉन होते हैं।
(e) इसके दूसरे कोश में पहले कोश की तुलना में दोगुने इलेक्ट्रॉन होते हैं ?
उत्तर:
(a) निऑन (2, 8)
(b) मैग्नीशियम
(c) सिलिकॉन (2, 8, 4)
(d) बोरॉन (2, 3)
(e) कार्बन (2, 4)
प्रश्न 4
(a) आवर्त सारणी के उसी स्तंभ के सभी तत्वों में बोरॉन के समान क्या गुण समान है?
(b) आवर्त सारणी के उसी स्तंभ के सभी तत्वों में फ्लोरीन के समान क्या गुण समान है?
उत्तर:
(a) बोरॉन के समान स्तंभ या समूह के तत्वों की संयोजकता तीन होती है और उनके पास तीन संयोजकता इलेक्ट्रॉन होते हैं।
(b) फ्लोरीन के समान स्तंभ या समूह के तत्व अम्लीय ऑक्साइड बनाते हैं और उनके सबसे बाहरी कोश में सात इलेक्ट्रॉन होते हैं और उनकी संयोजकता एक होती है।
प्रश्न 5
एक परमाणु का इलेक्ट्रॉनिक विन्यास 2, 8, 7 है।
(a) इस तत्व की परमाणु संख्या क्या है?
(b) निम्नलिखित में से किस तत्व के साथ यह रासायनिक रूप से समान होगा? (परमाणु संख्याएँ कोष्ठक में दी गई हैं।)
N (7), F (9), P (15), Ar (18)
उत्तर:
(a) दिए गए तत्व की परमाणु संख्या 2 + 8 + 7(= 17) है।
(b) यह रासायनिक रूप से फ्लोरीन [F(9)] के समान होगा क्योंकि इसका इलेक्ट्रॉनिक विन्यास 2, 7 है।
प्रश्न 6
नाइट्रोजन (परमाणु क्रमांक 7) और फॉस्फोरस (परमाणु क्रमांक 15) आवर्त सारणी के समूह 15 से संबंधित हैं। इन दोनों तत्वों का इलेक्ट्रॉनिक विन्यास लिखिए। इनमें से कौन अधिक विद्युत ऋणात्मक होगा? क्यों?
उत्तर:
नाइट्रोजन का इलेक्ट्रॉनिक विन्यास -2,5
फॉस्फोरस का इलेक्ट्रॉनिक विन्यास = 2, 8, 5
नाइट्रोजन अधिक विद्युत ऋणात्मक होगा क्योंकि सबसे बाहरी कोश नाभिक के निकट होता है और इसलिए नाभिक इलेक्ट्रॉनों को अधिक मजबूती से आकर्षित करेगा। आवर्त सारणी के एक समूह में, ऊपर से नीचे की ओर बढ़ने पर इलेक्ट्रॉन आकर्षित करने की प्रवृत्ति कम होती जाती है।
प्रश्न 7
किसी परमाणु का इलेक्ट्रॉनिक विन्यास आधुनिक आवर्त सारणी में उसकी स्थिति से कैसे संबंधित है?
उत्तर:
आधुनिक आवर्त सारणी परमाणु क्रमांक पर आधारित है और परमाणु क्रमांक सीधे इलेक्ट्रॉनिक विन्यास से संबंधित है। इलेक्ट्रॉनिक विन्यास के आधार पर किसी तत्व की समूह संख्या और आवर्त संख्या ज्ञात की जा सकती है। उदाहरण के लिए, यदि किसी तत्व के सबसे बाहरी कोश में 1 या 2 इलेक्ट्रॉन हैं, तो वह समूह 1 या समूह 2 से संबंधित होगा। और यदि उसके सबसे बाहरी कोश में 3 या अधिक इलेक्ट्रॉन हैं, तो वह समूह 10 से संबंधित होगा। 4- सबसे बाहरी कोश में इलेक्ट्रॉनों की संख्या।
सभी क्षार धातुओं के सबसे बाहरी कोश में एक इलेक्ट्रॉन होता है, इसलिए उन्हें समूह 1 में रखा गया है। इस प्रकार, समूह 2 के सभी तत्वों के सबसे बाहरी कोश में 2 इलेक्ट्रॉन होते हैं। समूह 15 के तत्वों के सबसे बाहरी कोश में 5 इलेक्ट्रॉन होते हैं। इसी प्रकार, किसी तत्व में कोशों की संख्या उसकी आवर्त संख्या दर्शाती है। उदाहरण के लिए, मैग्नीशियम का परमाणु क्रमांक 12 है और इसका इलेक्ट्रॉनिक विन्यास 2, 8, 2 है। इस प्रकार यह तीसरे आवर्त का तत्व है।
प्रश्न 8
आधुनिक आवर्त सारणी में, कैल्शियम (परमाणु क्रमांक 20) परमाणु क्रमांक 12, 19, 21 और 38 वाले तत्वों से घिरा हुआ है। इनमें से किसके भौतिक और रासायनिक गुण कैल्शियम के समान हैं?
उत्तर:
निम्न तत्वों का इलेक्ट्रॉनिक विन्यास:
परमाणु क्रमांक 12 = 2, 8, 2
परमाणु क्रमांक 19 = 2, 8, 8, 1
परमाणु क्रमांक 20 = 2, 8, 8, 2
परमाणु क्रमांक 21 = 2, 8, 9, 2
परमाणु क्रमांक 38 = 2, 8, 18, 8, 2
परमाणु क्रमांक 12 अर्थात मैग्नीशियम (Mg) और 38 अर्थात स्ट्रोंटियम (Sr) के भौतिक और रासायनिक गुण परमाणु क्रमांक 20 अर्थात कैल्शियम (Ca) वाले तत्व के समान होंगे।
कक्षा 10 विज्ञान अध्याय 5 तत्वों का आवर्त वर्गीकरण के लिए एनसीईआरटी समाधान
तत्वों का आवर्त वर्गीकरण: वर्गीकरण की आवश्यकताएँ, आधुनिक आवर्त सारणी, गुणों में क्रम, संयोजकता, परमाणु क्रमांक, धात्विक और अधात्विक गुण।
प्रश्न 1
क्या न्यूलैंड्स अष्टक के स्तंभों में भी डोबेरिनर त्रिक मौजूद थे? तुलना करके पता लगाएँ।
हल:
हाँ, न्यूलैंड्स अष्टक के स्तंभों में भी डोबेरिनर त्रिक मौजूद हैं। उदाहरण के लिए, न्यूलैंड्स वर्गीकरण के दूसरे स्तंभ में लिथियम (Li), सोडियम (Na) और पोटेशियम (K) तत्व हैं, जो एक डोबेरिनर त्रिक बनाते हैं।
प्रश्न 2
डोबेरेनर के वर्गीकरण की सीमाएँ क्या थीं?
समाधान:
सभी ज्ञात तत्वों को त्रिक के रूप में व्यवस्थित नहीं किया जा सका। बहुत कम द्रव्यमान या बहुत अधिक द्रव्यमान वाले तत्वों के लिए, डोबेरेनर त्रिक लागू नहीं होते। F, Cl और Br का उदाहरण लें। Cl का परमाणु द्रव्यमान, F और Br के परमाणु द्रव्यमानों का अंकगणितीय माध्य नहीं है। जैसे-जैसे परमाणु द्रव्यमानों को सटीक रूप से मापने की तकनीकें विकसित होती गईं, डोबेरेनर त्रिक पूरी तरह से मान्य नहीं रह पाया।
प्रश्न 3
न्यूलैंड के अष्टक नियम की सीमाएँ क्या थीं?
हल:
यह नियम उन तत्वों के लिए मान्य नहीं था जिनका परमाणु द्रव्यमान Ca से अधिक था। जब और तत्वों की खोज हुई, जैसे कि He, Ne, Ar जैसे उत्कृष्ट गैसों से बने तत्व, तो उन्हें उनकी तालिका में शामिल नहीं किया जा सका।
प्रश्न 4
मेंडेलीव की आवर्त सारणी का उपयोग करके निम्नलिखित तत्वों के ऑक्साइडों के सूत्रों की भविष्यवाणी करें: K, C, Al, Si, Ba.
हल:
K 2 O – पोटेशियम ऑक्साइड
CaO – कैल्शियम ऑक्साइड
Al 2 O 3 – एल्युमिनियम ऑक्साइड
SiO 2 – सिलिकॉन डाइऑक्साइड
BaO – बेरियम ऑक्साइड.
प्रश्न 5
गैलियम के अलावा, मेंडेलीव ने अपनी आवर्त सारणी में किन अन्य तत्वों को उनकी खोज के बाद से छोड़ दिया है? (कोई दो)
समाधान:
स्कैंडियम और जर्मेनियम।
प्रश्न 6
मेंडेलीव ने अपनी आवर्त सारणी बनाने में किन मानदंडों का इस्तेमाल किया?
उत्तर:
उन्होंने तत्वों के परमाणु द्रव्यमान और उनके भौतिक गुणों के बीच संबंध का अवलोकन किया। रासायनिक गुणों में, उन्होंने ऑक्सीजन और हाइड्रोजन के साथ तत्वों द्वारा निर्मित यौगिकों पर ध्यान केंद्रित किया।
प्रश्न 7
आपके विचार से उत्कृष्ट गैसों को एक अलग समूह में क्यों रखा गया है?
उत्तर:
हमारे वायुमंडल में इनकी निष्क्रियता और कम सांद्रता के कारण, इन्हें मौजूदा क्रम में बिना किसी बदलाव के एक नए समूह में रखा जा सकता है।
प्रश्न 8
आधुनिक आवर्त सारणी मेंडेलीव की आवर्त सारणी की विभिन्न विसंगतियों को कैसे दूर कर सकती है?
समाधान:
जब तत्वों को आधुनिक आवर्त नियम के आधार पर उनकी परमाणु संख्याओं के अनुसार व्यवस्थित किया जाता है, तो मेंडेलीव के वर्गीकरण की सभी विसंगतियाँ (दोष) दूर हो जाती हैं। उदाहरण के लिए, समस्थानिकों की स्थिति: किसी तत्व के सभी समस्थानिकों में प्रोटॉन की संख्या समान होती है, इसलिए उनकी परमाणु संख्या भी समान होती है। चूँकि किसी तत्व के सभी समस्थानिकों की परमाणु संख्या समान होती है, इसलिए उन्हें आवर्त सारणी के एक ही समूह में एक स्थान पर रखा जा सकता है।
प्रश्न 9
दो ऐसे तत्वों के नाम बताइए जिनसे आप मैग्नीशियम के समान रासायनिक अभिक्रियाएँ प्रदर्शित करने की अपेक्षा करते हैं। आपके चयन का आधार क्या है?
हल:
कैल्शियम और बेरिलियम ऐसे तत्व हैं जो मैग्नीशियम के समान रासायनिक अभिक्रियाएँ प्रदर्शित करेंगे। ऐसा इसलिए है क्योंकि बेरिलियम और कैल्शियम, आवर्त सारणी के उसी समूह से संबंधित हैं जिसमें मैग्नीशियम है। इन सभी का इलेक्ट्रॉनिक विन्यास समान है और प्रत्येक में 2 संयोजकता इलेक्ट्रॉन हैं।
प्रश्न 10
नाम:
a. तीन तत्व जिनके सबसे बाहरी शेल में एक इलेक्ट्रॉन होता है।<
b. दो तत्व जिनके सबसे बाहरी शेल में दो इलेक्ट्रॉन होते हैं।<
c. भरे हुए बाहरी शेल वाले तीन तत्व।
हल:
a. तीन तत्व जिनके सबसे बाहरी शेल में एक इलेक्ट्रॉन होता है:
1. लिथियम
2. सोडियम
3. पोटेशियम
b. दो तत्व जिनके सबसे बाहरी शेल में दो इलेक्ट्रॉन होते हैं:
1. मैग्नीशियम
2. कैल्शियम
c. भरे हुए बाहरी शेल वाले तीन तत्व:
1. आर्गन
2. हीलियम
3. निऑन।
प्रश्न 11
a. लिथियम, सोडियम, पोटेशियम ऐसी धातुएँ हैं जो जल के साथ अभिक्रिया करके हाइड्रोजन मुक्त करती हैं। क्या इन तत्वों के परमाणुओं में कोई समानता है?
b. हीलियम एक अक्रियाशील गैस है और नियॉन अत्यंत कम अभिक्रियाशीलता वाली गैस है। यदि कुछ है, तो उनके परमाणुओं में क्या समानता है?
उत्तर:
a. ये तत्व क्षार धातुएँ हैं और इनके सबसे बाहरी कोश में 1 संयोजकता इलेक्ट्रॉन होता है और इसलिए ये बहुत अस्थिर और क्रियाशील होते हैं।
b. इन तत्वों में से प्रत्येक का सबसे बाहरी उपकोश पूर्ण होता है, जिसके परिणामस्वरूप उच्च स्थिरता होती है। ये केवल चरम परिस्थितियों में ही अन्य तत्वों के साथ अभिक्रिया करते हैं, जिस गुण के लिए इन्हें यह नाम दिया गया है।
प्रश्न 12
आधुनिक आवर्त सारणी में पहले दस तत्वों में कौन-सी धातुएँ हैं?
उत्तर:
ये धातुएँ लिथियम और बेरिलियम हैं।
प्रश्न 13
आवर्त सारणी में उनकी स्थिति को ध्यान में रखते हुए, आप निम्नलिखित में से किस तत्व में अधिकतम धात्विक विशेषता की अपेक्षा करेंगे?
Ga, Ge, As, Se, Be
हल:
बेरिलियम
प्रश्न 14
आवर्त सारणी के आवर्तों में बाएं से दाएं जाने पर प्रवृत्तियों के बारे में निम्नलिखित में से कौन सा कथन सही नहीं है?<
(i)तत्व प्रकृति में कम धात्विक हो जाते हैं
(ii) संयोजकता इलेक्ट्रॉनों की संख्या बढ़ जाती है
(iii) परमाणु अपने इलेक्ट्रॉनों को अधिक आसानी से खो देते हैं
(iv) ऑक्साइड अधिक अम्लीय हो जाते हैं
समाधान:
(iii) परमाणु अपने इलेक्ट्रॉनों को अधिक आसानी से खो देते हैं - गलत कथन।
प्रश्न 15
किस तत्व में है?
a. दो कोश, जिनमें से दोनों पूरी तरह से इलेक्ट्रॉनों से भरे हुए हैं? <
b. 2,8,2 का इलेक्ट्रॉनिक विन्यास? <
c. कुल तीन कोश, जिसके संयोजकता कोश में चार इलेक्ट्रॉन हैं? <
d. कुल दो कोश, जिसके संयोजकता कोश में तीन इलेक्ट्रॉन हैं? <
e. इसके दूसरे कोश में पहले कोश की तुलना में दोगुने इलेक्ट्रॉन हैं?
हल:
a. निऑन (2,8)
b. मैग्नीशियम (2,8,2)
c. सिलिकॉन (2,8,4)
d. बोरॉन (2,3)
e. कार्बन (2,4)
प्रश्न 16
आवर्त सारणी के फ्लोरीन जैसे स्तंभ के सभी तत्वों में कौन-सा गुण समान है?
उत्तर:
इन सभी तत्वों के सबसे बाहरी कोश में 7 इलेक्ट्रॉन होते हैं और ये प्रायः क्षार धातु समूह के तत्वों के साथ लवण के रूप में संयुक्त होते हैं।
प्रश्न 17
एक परमाणु का इलेक्ट्रॉनिक विन्यास 2,8,7 है।
i. इस तत्व का परमाणु क्रमांक क्या है?
ii. यह निम्नलिखित में से किस तत्व के साथ रासायनिक रूप से समान होगा<
N (7) F (9) P (15) Ar (18)
हल:
(i) क्लोरीन - 17
(ii) F (9)
प्रश्न 18
तत्व A द्वारा किस प्रकार का आयन, धनायन या ऋणायन, बनेगा?
हल:
C, A से कम अभिक्रियाशील है।
आवर्त में आगे बढ़ने पर परमाणु आकार घटने के कारण “C” का आकार “B” से छोटा होगा।
तत्व A द्वारा ऋणायन बनेगा।
प्रश्न 19
नाइट्रोजन (परमाणु क्रमांक 7) और फॉस्फोरस (परमाणु क्रमांक 15) आवर्त सारणी के समूह 15 से संबंधित हैं। इन दोनों तत्वों का इलेक्ट्रॉनिक विन्यास लिखिए। इनमें से कौन अधिक विद्युत ऋणात्मक होगा? क्यों?
हल:
इलेक्ट्रॉनिक विन्यास - नाइट्रोजन - 2s 2 2p 3 और फॉस्फोरस - 1s 2 2s 2 2p 6 3s 2 3p 3। नाइट्रोजन अधिक विद्युत ऋणात्मक होगा; ऐसा इसलिए है क्योंकि इसके परमाणु का आकार छोटा होता है जिसके कारण आने वाले इलेक्ट्रॉन के लिए इसके नाभिक का आकर्षण अधिक होता है।
प्रश्न 20
किसी परमाणु का इलेक्ट्रॉनिक विन्यास आधुनिक आवर्त सारणी में उसकी स्थिति से किस प्रकार संबंधित है?
उत्तर:
किसी परमाणु का इलेक्ट्रॉनिक विन्यास उसके सबसे बाहरी संयोजकता कोश में बढ़ता है जो आधुनिक आवर्त सारणी में उसकी स्थिति से संबंधित है।
प्रश्न 21
आधुनिक आवर्त सारणी में, कैल्शियम (परमाणु क्रमांक 20) परमाणु क्रमांक 12, 19, 21 और 38 वाले तत्वों से घिरा हुआ है। इनमें से किन तत्वों के भौतिक और रासायनिक गुण कैल्शियम के समान हैं?
उत्तर:
कैल्शियम का परमाणु क्रमांक 20 है, इसलिए इसका इलेक्ट्रॉनिक विन्यास 2, 8, 8, 2 है। इस प्रकार, कैल्शियम में 2 संयोजकता इलेक्ट्रॉन होते हैं (इसके सबसे बाहरी कोश में)। अब, जिस तत्व में 2 संयोजकता इलेक्ट्रॉन होंगे, उसके भौतिक और रासायनिक गुण कैल्शियम के समान होंगे। परमाणु क्रमांक 12 वाले तत्व का इलेक्ट्रॉनिक विन्यास 2, 8, 2 है। इसमें कैल्शियम की तरह ही 2 संयोजकता इलेक्ट्रॉन होते हैं। इसलिए, परमाणु क्रमांक 12 वाले तत्व के भौतिक और रासायनिक गुण कैल्शियम के समान होंगे।
प्रश्न 22
आपके विचार से आधुनिक आवर्त सारणी में हाइड्रोजन को कहाँ रखा जाना चाहिए?
उत्तर:
हाइड्रोजन तत्व को समूह 1 में सबसे ऊपर, क्षार धातुओं से ऊपर रखा गया है क्योंकि हाइड्रोजन का इलेक्ट्रॉनिक विन्यास क्षार धातुओं के समान है।
बहुविकल्पीय प्रश्न (MCQs) [प्रत्येक 1 अंक]
प्रश्न 1.
निम्नलिखित में से कौन सा दूसरे आवर्त के तत्वों के लिए सबसे बाहरी कोश है? [एनसीईआरटी उदाहरण]
(a) K-कोश
(b) L-कोश
(c) M-कोश
(d) N-कोश
उत्तर:
(b) दूसरे आवर्त के तत्वों में दूसरा कोश, अर्थात् Z-कोश भरा होता है। क्योंकि दूसरे आवर्त में दो कोश, K और L होते हैं।
प्रश्न 2.
एक तत्व जो सभी कार्बनिक यौगिकों का एक आवश्यक घटक है, वह किससे संबंधित है? [एनसीईआरटी उदाहरण]
(ए) समूह 1
(बी) समूह 14
(सी) समूह 15
(डी) समूह 16
उत्तर:
(बी) सभी कार्बनिक यौगिकों का घटक कार्बन है। यह समूह 14 से संबंधित है।
प्रश्न 3.
निम्नलिखित में से कौन सा तत्व अधिकतम संख्या में संयोजकता इलेक्ट्रॉन प्रदर्शित करता है? [एनसीईआरटी उदाहरण]
(a) Na
(b) Al
(c) Si
(d) P
उत्तर:
(d) Na (समूह 1) में एक, A1 (समूह 13) में तीन (13 -10), Si (समूह 14) में चार (14-10) और P (समूह 15) में पाँच (15 - 10) संयोजकता इलेक्ट्रॉन हैं। इसलिए, P में संयोजकता इलेक्ट्रॉनों की संख्या अधिकतम है, अर्थात 3 (दिए गए तत्वों में अधिकतम)।
प्रश्न 4.
दिए गए तत्वों A, B, C, D और E में से कौन से तत्व क्रमशः परमाणु क्रमांक 2, 3, 7, 10 और 30 के साथ एक ही आवर्त में हैं? [एनसीईआरटी उदाहरण]
(a) A, B, C
(b) B, C, D
(c) A, D, E
(d) B, D, E
उत्तर:
(b) दूसरे आवर्त में परमाणु क्रमांक 3(Li), 7(N), 10(Ne) वाले तत्व होते हैं। चूँकि, दूसरे आवर्त में परमाणु क्रमांक 3 से 10 तक के तत्व होते हैं।
प्रश्न 5.
तत्वों A, B, C, D और E के परमाणु क्रमांक क्रमशः 9, 11, 17, 12 और 13 हैं। तत्वों का कौन सा युग्म एक ही समूह से संबंधित है? [एनसीईआरटी उदाहरण]
(a) A और B
(b) B और D
(c) A और C
(d) D और E
उत्तर:
(c)A (परमाणु क्रमांक = 9) का इलेक्ट्रॉनिक विन्यास 2, 7 है।
B (परमाणु क्रमांक = 11) का इलेक्ट्रॉनिक विन्यास 2, 8, 1 है।
C (परमाणु संख्या = 17) का इलेक्ट्रॉनिक विन्यास 2, 8, 7 है।
D (परमाणु संख्या = 12) का इलेक्ट्रॉनिक विन्यास 2, 8, 2 है।
E (परमाणु संख्या = 13) का इलेक्ट्रॉनिक विन्यास 2, 8, 3 है।
वे तत्व जिनकी परमाणु संख्या में 8 का अंतर है, अर्थात् 9 (A, फ्लोरीन) और 17 (C, क्लोरीन) एक ही समूह में आते हैं, अर्थात् समूह 17 (हैलोजन)।
प्रश्न 6.
मेंडलीफ की आवर्त सारणी में बाद में खोजे जाने वाले तत्वों के लिए रिक्त स्थान छोड़े गए थे। निम्नलिखित में से किस तत्व को आवर्त सारणी में बाद में स्थान मिला? [एनसीईआरटी उदाहरण]
(a) जर्मेनियम
(b) क्लोरीन
(c) ऑक्सीजन
(d) सिलिकॉन
उत्तर:
(a) मेंडलीफ ने आवर्त सारणी में उन तत्वों के लिए कुछ रिक्त स्थान छोड़े थे जो उस समय ज्ञात नहीं थे। जर्मेनियम तत्व को आवर्त सारणी में बाद में स्थान मिला और मेंडलीफ की भविष्यवाणियाँ उल्लेखनीय रूप से सही पाई गईं।
प्रश्न 7.
निम्नलिखित में से कौन से तत्व के समस्थानिकों की विशेषताएँ हैं? [एनसीईआरटी उदाहरण]
(i) एक तत्व के समस्थानिकों के परमाणु द्रव्यमान समान होते हैं।
(ii) एक तत्व के समस्थानिकों की परमाणु संख्या समान होती है।
(iii) एक तत्व के समस्थानिक समान भौतिक गुण प्रदर्शित करते हैं।
(iv) एक तत्व के समस्थानिक समान रासायनिक गुण प्रदर्शित करते हैं।
(a) (i), (iii) और (iv)
(b) (ii), (iii) और (iv)
(c) (ii) और (iii)
(d) (ii) और (iv)
उत्तर:
(d) एक तत्व के समस्थानिकों की परमाणु संख्या समान होती है और वे समान रासायनिक गुण प्रदर्शित करते हैं।
प्रश्न 8.
निम्नलिखित में से कौन सा तत्व आसानी से इलेक्ट्रॉन खो देगा? [एनसीईआरटी उदाहरण]
(ए) एमजी
(बी) ना
(सी) के
(डी) सीए
उत्तर:
(सी) एमजी का इलेक्ट्रॉनिक विन्यास (परमाणु संख्या = 12) 2, 8, 2
ना का इलेक्ट्रॉनिक विन्यास (परमाणु संख्या = 11) 2, 8, 1
K का इलेक्ट्रॉनिक विन्यास (परमाणु संख्या = 19) 2, 8, 8, 1
सीए का इलेक्ट्रॉनिक विन्यास (परमाणु संख्या = 20) 2, 8, 8, 2
उपरोक्त इलेक्ट्रॉनिक विन्यासों से, यह स्पष्ट है कि K और Na स्थिर विन्यास प्राप्त करने के लिए आसानी से इलेक्ट्रॉन खो देंगे। लेकिन K और Na में से, K अधिक आसानी से इलेक्ट्रॉन खो देगा क्योंकि K के वैलेंस इलेक्ट्रॉन पर आकर्षण बल दिए गए तत्वों में सबसे कम है।
प्रश्न 9.
निम्नलिखित में से किस तत्व की परमाणु त्रिज्या सबसे अधिक है? [एनसीईआरटी उदाहरण]
(a) Na
(b) Mg
(c) K
(d) Ca
उत्तर:
(c) किसी समूह में नीचे जाने पर परमाणु त्रिज्या बढ़ती है। Na और K एक ही समूह में हैं और K, Na से नीचे है, इसलिए K की परमाणु त्रिज्या अधिक होगी, अर्थात K > Na। किसी आवर्त में बाएँ से दाएँ जाने पर परमाणु त्रिज्या घटती है। चूँकि, K और Ca एक ही आवर्त में हैं और K पहले समूह में है और Ca दूसरे समूह में है, इसलिए K की परमाणु त्रिज्या Ca से अधिक होगी, अर्थात K > Ca।
साथ ही Na और Mg एक ही आवर्त में हैं, लेकिन Na पहले समूह से संबंधित है और Mg दूसरे समूह से संबंधित है, इसलिए Na की परमाणु त्रिज्या Mg से अधिक है, अर्थात Na > Mg। इस प्रकार, यदि हम इन सभी को एक साथ लें तो हमें K > Na >Mg और K > Ca > Mg प्राप्त होता है। इसलिए, हम कह सकते हैं कि K की परमाणु त्रिज्या सबसे बड़ी है।
प्रश्न 10.
आवर्त सारणी के आवर्तों में बाएँ से दाएँ जाने पर प्रवृत्तियों के बारे में निम्नलिखित में से कौन सा कथन सही नहीं है? [एनसीईआरटी]
(a) तत्वों की प्रकृति कम धात्विक हो जाती है
(b) संयोजकता इलेक्ट्रॉनों की संख्या बढ़ जाती है
(c) परमाणु अपने इलेक्ट्रॉनों को अधिक आसानी से खो देते हैं
(d) ऑक्साइड अधिक अम्लीय हो जाते हैं
उत्तर:
(c) बाएँ से दाएँ जाने पर परमाणु क्रमांक बढ़ता है और इसलिए, आवेश बढ़ता है। आवेश बढ़ने के साथ, इलेक्ट्रॉन को बांधने वाला बल बढ़ता है, इसलिए परमाणु आसानी से नहीं, बल्कि अधिक कठिनाई से इलेक्ट्रॉनों को खोते हैं।
प्रश्न 11.
निम्नलिखित में से कौन सा एक परमाणु की परमाणु त्रिज्या (r) का सही निरूपण करता है? [एनसीईआरटी उदाहरण]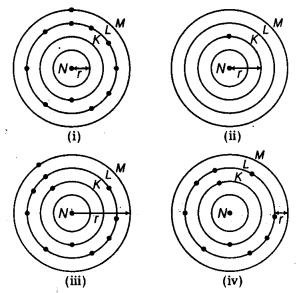
(a) (i) और (i)
(b) (ii) और (iii)
(c) (iii) और (iv)
(d) (i) और (iv)
उत्तर:
(b) परमाणु त्रिज्या नाभिक और बाहरी कक्षा [जिसमें इलेक्ट्रॉन होते हैं] के बीच की दूरी है। अतः (ii) और (iii) सही निरूपण हैं।
प्रश्न 12.
आधुनिक आवर्त सारणी के बारे में निम्नलिखित में से कौन सा/से कथन गलत है/हैं?
(i) आधुनिक आवर्त सारणी में तत्वों को उनकी घटती परमाणु संख्या के आधार पर व्यवस्थित किया गया है।
(ii) आधुनिक आवर्त सारणी में तत्वों को उनके बढ़ते परमाणु द्रव्यमान के आधार पर व्यवस्थित किया गया है।
(iii) समस्थानिकों को आवर्त सारणी में आसन्न समूह में रखा गया है।
(iv) आधुनिक आवर्त सारणी में तत्वों को उनकी बढ़ती परमाणु संख्या के आधार पर व्यवस्थित किया गया है। [एनसीईआरटी उदाहरण]
(a) केवल (i)
(b) (i), (ii) और (iii)
(c) (i), (ii) और (iv)
(d) केवल (iv)
उत्तर:
(b) केवल कथन (iv) सही है। आधुनिक आवर्त सारणी में सभी तत्वों को उनकी बढ़ती परमाणु संख्या के आधार पर व्यवस्थित किया गया है। सभी समस्थानिकों को आवर्त सारणी के एक ही समूह में एक स्थान पर रखा जा सकता है।
प्रश्न 13.
परमाणु क्रमांक 14 वाला तत्व कठोर है और अम्लीय ऑक्साइड तथा सहसंयोजक हैलाइड बनाता है। यह तत्व निम्नलिखित में से किस श्रेणी में आता है? [एनसीईआरटी उदाहरण]
(a) धातु
(b) उपधातु
(c) अधातु
(d) बाएँ पक्ष का तत्व
उत्तर:
(c) इसके सबसे बाहरी कोश में 4 इलेक्ट्रॉन हैं। अतः यह एक अधातु है। अधातु अम्लीय ऑक्साइड बनाती है और हैलोजन के साथ इलेक्ट्रॉनों की साझेदारी करके सहसंयोजक हैलाइड बनाती है।
प्रश्न 14.
निम्नलिखित तत्वों को उनके घटते धात्विक गुण के क्रम में व्यवस्थित करें Na, Si, Cl, Mg, Al। [एनसीईआरटी उदाहरण]
(a) Cl > Si > Al > Mg > Na
(b) Na > Mg > Al > Si > Cl
(c) Na > Al > Mg > Cl > Si
(d) Al > Na > Si > Ca > Mg
उत्तर:
(b) धातुएँ आवर्त सारणी के सबसे बाईं ओर होती हैं। एक आवर्त में बाएँ से दाएँ जाने पर धात्विक गुण घटता है। Na, Si, Cl, Mg, Al, Na, Mg, Al, Si, Cl के क्रम में समान आवर्त के हैं। एक आवर्त में बाएँ से दाएँ जाने पर धात्विक गुण घटता है। इस प्रकार, धात्विक गुण घटने का क्रम है: Na > Mg > Al > Si > Cl
प्रश्न 15.
निम्नलिखित में से तत्वों का कौन सा समूह उनके बढ़ते धात्विक गुण के क्रम में लिखा गया है? [एनसीईआरटी उदाहरण]
(a) Be, Mg, Ca
(b) Na, Li, K
(c) Mg, Al, Si
(d) C, O, N
उत्तर:
(a) समूह में नीचे जाने पर धात्विक गुण बढ़ता है।
प्रश्न 16.
आवर्त सारणी के समूह में नीचे जाने पर निम्नलिखित में से कौन सा नहीं बढ़ता है? [एनसीईआरटी उदाहरण]
(ए) परमाणु त्रिज्या
(बी) धात्विक गुण
(सी) वैलेंस इलेक्ट्रॉन
(डी) एक तत्व में गोले की संख्या
उत्तर:
(सी) प्रत्येक समूह में तत्वों में कुछ संख्या में वैलेंस इलेक्ट्रॉन होते हैं इसलिए उनकी वैलेंस समान होती है और इस प्रकार वे समान रासायनिक गुण प्रदर्शित करते हैं।
प्रश्न 17.
निम्नलिखित में से कौन सा तत्व अम्लीय ऑक्साइड बनाएगा? [एनसीईआरटी उदाहरण]
(ए) एक तत्व जिसका परमाणु क्रमांक = 7 है
(बी) एक तत्व जिसका परमाणु क्रमांक = 3 है
(सी) एक तत्व जिसका परमाणु क्रमांक = 12 है
(डी) एक तत्व जिसका परमाणु क्रमांक = 19 है
उत्तर:
(ए) गैर-धातु सामान्य रूप से अम्लीय ऑक्साइड बनाते हैं। गैर-धातुओं में सबसे बाहरी शेल में 4 से 8 इलेक्ट्रॉन होते हैं। दिए गए तत्वों का इलेक्ट्रॉनिक विन्यास (ए) यानी 7 = 2, 5 (बी) यानी 3 = 2, 1 (सी) यानी 12 = 2, 8, 2 (डी) यानी 19 = 2, 8, 8,1 है।
तो, परमाणु संख्या = 7 (इलेक्ट्रॉनिक विन्यास = 2, 5) वाला तत्व गैर-धातु (एन) है और यह एक अम्लीय ऑक्साइड बनाएगा। शेष तीन तत्व जिनकी परमाणु संख्या 3 (Li), 12 (Mg) और 19 (K) है, धातु हैं और इसलिए क्षारीय ऑक्साइड बनाते हैं।
प्रश्न 18.
एका-एल्युमीनियम किस प्रकार का ऑक्साइड बनाएगा? [एनसीईआरटी उदाहरण]
(a) EO 3
(b) E 3 O 2
(C) E 2 O 3
(d) EO
उत्तर: (c) गैलियम की संयोजकता 3 है। इसलिए, यह आणविक सूत्र E 2 O 3
वाला ऑक्साइड बनाता है । अन्य विकल्पों में, E की संयोजकता 3 नहीं है।
प्रश्न 19.
संलग्न आरेख एक तत्व (जिसकी संयोजकता = 4 है) के परमाणुओं की व्यवस्था को दर्शाता है जो विशाल सहसंयोजक नेटवर्क बनाते हैं।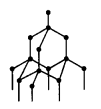
उस भारी धातु की पहचान कीजिए जो ऊपर चर्चा किए गए तत्व के समान समूह से संबंधित है।
(a) As
(b) Bi
(c) Pb
(d) Hg
उत्तर:
(c) आरेख में चर्चा किया गया तत्व कार्बन है। कार्बन (C) और लेड (Pb) दोनों समूह IVA से संबंधित हैं।
प्रश्न 20.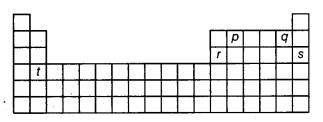
आवर्त सारणी की ऊपर दिखाई गई रूपरेखा में अक्षरों p, q, r, s और t द्वारा दर्शाए गए तत्वों को उनकी संयोजकता के बढ़ते क्रम में व्यवस्थित करें।
(a) t < q < r < s < p
(b) s < t < q < r < p
(c) s < q < t < r < p
(d) q < s < t < p < r
उत्तर:
(c) p(समूह IVA), q(समूह VIIA), r(समूह IILA) s(समूह VIII) और t(समूह IIA) की संयोजकता क्रमशः 4, 1, 3, 0 और 2 है इसलिए बढ़ती संयोजकता का सही क्रम है: s(0) < q(1) < t(2) < r(3) < p(4)
प्रश्न 21.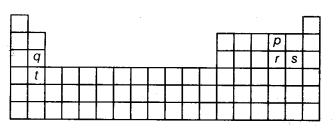
ऊपर दिया गया चित्र आवर्त सारणी की रूपरेखा दर्शाता है। अक्षर p, q, r, s और t तत्वों को दर्शाते हैं। निम्नलिखित में से कौन-सा अक्षर युग्म उन तत्वों को दर्शाता है जिनके परमाणु में समान संख्या में कोश होते हैं?
(a) p और q
(b) r और t
(c) p और s
(d) g और s
उत्तर:
(d) तत्व q और s आवर्त सारणी के समान आवर्त से संबंधित हैं और इसलिए, उनके कोशों की संख्या भी समान होगी।
