NCERT Class 9 Science Chapter 3 परमाणु एवं अणु
NCERT Solutions For Class 9 Science Chapter 3 परमाणु एवं अणु
पाठ्य में हल किए गए प्रश्न
पाठ्य प्रश्नों में
प्रश्न 1.
एक प्रतिक्रिया में, 5.3 ग्राम सोडियम कार्बोनेट ने 6.0 ग्राम एथेनोइक एसिड के साथ प्रतिक्रिया की। उत्पाद 2.2 ग्राम कार्बन डाइऑक्साइड, 0.9 ग्राम पानी और 8.2 ग्राम सोडियम एथेनोएट थे। दिखाएं कि ये अवलोकन द्रव्यमान के संरक्षण के नियम के अनुरूप हैं। (सीबीएसई 2012)
उत्तर:
उत्पादों के लिए रासायनिक प्रतिक्रिया है:
सोडियम कार्बोनेट + एथेनोइक एसिड —> सोडियम एथेनोएट + कार्बन डाइऑक्साइड + पानी।
अभिकारकों का द्रव्यमान = (5.3 + 6.0) = 1.3 ग्राम
उत्पादों का द्रव्यमान = (8.2 + 2.2 + 0.9) = 11.3 ग्राम।
अभिकारकों और उत्पादों का द्रव्यमान समान है। इसका मतलब है कि प्रतिक्रिया के दौरान द्रव्यमान का कोई नुकसान नहीं हुआ था। इसलिए, डेटा द्रव्यमान के संरक्षण के नियम के अनुरूप है।
प्रश्न 2.
हाइड्रोजन और ऑक्सीजन द्रव्यमान के अनुसार 1:8 के अनुपात में संयोजित होकर जल बनाते हैं। 3 ग्राम हाइड्रोजन गैस के साथ अभिक्रिया करने के लिए ऑक्सीजन गैस के कितने द्रव्यमान की आवश्यकता होगी?
उत्तर:
उपलब्ध आँकड़ों के अनुसार,
1 ग्राम हाइड्रोजन के साथ संयोजित ऑक्सीजन का द्रव्यमान = 8 ग्राम।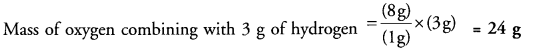
प्रश्न 3:
डाल्टन के परमाणु सिद्धांत का कौन सा अभिधारणा द्रव्यमान संरक्षण नियम का आधार है? (सीबीएसई 2012)
उत्तर:
द्रव्यमान संरक्षण नियम डाल्टन के परमाणु सिद्धांत के निम्नलिखित अभिधारणा पर आधारित है।
"भौतिक परिवर्तन या रासायनिक अभिक्रिया के दौरान परमाणुओं का न तो सृजन हो सकता है और न ही विनाश।"
प्रश्न 4.
डाल्टन के परमाणु सिद्धांत का कौन सा अभिधारणा निश्चित अनुपात के नियम की व्याख्या कर सकता है?
उत्तर:
निश्चित अनुपात का नियम डाल्टन के परमाणु सिद्धांत के निम्नलिखित अभिधारणा पर आधारित है।
"किसी विशेष तत्व के सभी परमाणु हर दृष्टि से समान होते हैं। इसका अर्थ है कि उनका द्रव्यमान, आकार और रासायनिक गुण समान होते हैं।"
प्रश्न 5.
परमाणु द्रव्यमान इकाई को परिभाषित कीजिए।
उत्तर:
परमाणु द्रव्यमान इकाई को इस प्रकार परिभाषित किया जा सकता है:
कार्बन के एक परमाणु के द्रव्यमान के बारहवें (1/12) भाग का द्रव्यमान 12 u के रूप में लिया जाता है। इसे 1 u (एकीकृत द्रव्यमान) के रूप में दर्शाया जाता है।
प्रश्न 6.
परमाणु को नंगी आँखों से देखना क्यों संभव नहीं है?
उत्तर:
परमाणु का आकार अत्यंत छोटा होने के कारण उसे नंगी आँखों से देखना संभव नहीं है। उदाहरण के लिए, हाइड्रोजन के एक परमाणु की त्रिज्या 10 -10 मीटर के क्रम की होती है। वास्तव में, परमाणु को एक सूक्ष्म कण माना जाता है। इन सूक्ष्म कणों को नंगी आँखों से नहीं देखा जा सकता।
प्रश्न 7.
इनके सूत्र लिखिए:
(i) सोडियम ऑक्साइड
(ii) एल्युमिनियम क्लोराइड
(iii) सोडियम सल्फाइड
(iv) मैग्नीशियम हाइड्रॉक्साइड।
उत्तर:
प्रश्न 8.
निम्नलिखित सूत्रों द्वारा प्रदर्शित यौगिकों के नाम लिखिए:
(i) Al2(SO4)3
(ii) CaCl2
(Hi) K2SO4
(iv) KNO3
(v) CaCO3.
उत्तर:
(i) एल्युमिनियम सल्फेट
(ii) कैल्शियम क्लोराइड
(iii) पोटेशियम सल्फेट
(iv) पोटेशियम नाइट्रेट
(v) कैल्शियम कार्बोनेट
रासायनिक सूत्र शब्द का क्या अर्थ है?
उत्तर:
अणु दो या दो से अधिक परमाणुओं (समान या भिन्न) के समूह को दर्शाता है जो रासायनिक रूप से एक-दूसरे से बंधे होते हैं और प्रबल आकर्षण बलों द्वारा एक-दूसरे से मजबूती से जुड़े होते हैं। अणुओं को उनके निर्माण करने वाले परमाणुओं के प्रतीकों द्वारा दर्शाया जाता है और इसे रासायनिक सूत्र कहते हैं।
इनके आणविक द्रव्यमानों की गणना करें:
(i) H 2
(ii) O 2
(iii) Cl 2
( iv) CO 2
(v) CH 4
(vi) C 2 H 6
(vii) C 2 H 4
(viii) NH 3
(ix) CH 3 OH।
उत्तर:
(i) हाइड्रोजन (H 2 ) H 2
का आणविक द्रव्यमान= 2 x H का परमाणु द्रव्यमान = (2 x 1 u) = 2 u। (ii) ऑक्सीजन (O 2 ) O 2 का आणविक द्रव्यमान= 2 x O का परमाणु द्रव्यमान = (2 x 16 u) = 32 u। (iii) क्लोरीन (CI 2 ) Cl 2 का आणविक द्रव्यमान = 2 x Cl का परमाणु द्रव्यमान = (2 x 35'5 u) = 71 u। (iv) कार्बन डाइऑक्साइड (CO 2 ) CO 2 का आणविक द्रव्यमान= (1 x C का परमाणु द्रव्यमान) + (2 x O का परमाणु द्रव्यमान) = (1 x 12 u) + (2 x 16 u) = 12 u + 32 u = 44 u. (v) मीथेन (CH 4 ) CH 4 का आणविक द्रव्यमान = (1 x C का परमाणु द्रव्यमान) + (4 x H का परमाणु द्रव्यमान) = (1 x 12 u) + (4 x 1 u) = 16 u. (vi) ईथेन (C 2 H 6 ) C 2 H 6 का आणविक द्रव्यमान= (2 x C का परमाणु द्रव्यमान) + (6 x H का परमाणु द्रव्यमान) = (2 x 12 u) + (6 x 1 u) = 30 u. (vii) एथिलीन (C 2 H 4 ) C 2 H 4 का आणविक द्रव्यमान= (2 x C का परमाणु द्रव्यमान) + (4 x H का परमाणु द्रव्यमान) = (2 x 12 u) + (4 x 1 u) = 28 u. (viii) अमोनिया (NH 3 ) NH 3 का आणविक द्रव्यमान = (1 x N का परमाणु द्रव्यमान) + (3 x H का परमाणु द्रव्यमान) = (1 x 14 u) + (3 x 1 u) = 17 u. (ix) मिथाइल अल्कोहल (CH 3 OH) CH 3 OH का आणविक द्रव्यमान= (1 x C का परमाणु द्रव्यमान) + (4 x H का परमाणु द्रव्यमान) + (1 x O का परमाणु द्रव्यमान) = (1 x 12 u) + (4 x 1 u) + (1 x 16 u) = 32 u.
इनके सूत्र इकाई द्रव्यमान की गणना करें:
(i) ZnO(
ii) Na 2 O
(iii) K 2 CO 3।
दिया गया है: Zn के परमाणु द्रव्यमान = 65 u, Na = 23 u, K = 39 u, C = 12 u और O = 16 u।
उत्तर:
(i) ZnO (जिंक ऑक्साइड) का सूत्र इकाई द्रव्यमान
= (1 x Zn का परमाणु द्रव्यमान) + (1 x O का परमाणु द्रव्यमान)
= (1 x 65 u) + (1 x 16 u) = 81 u। (ii) Na 2 O (सोडियम ऑक्साइड)
का सूत्र इकाई द्रव्यमान = (2 x Na का परमाणु द्रव्यमान) + (1 x O का परमाणु द्रव्यमान) = (2 x 23 u) + (1 x 16 u) = 62 u। (iii) K 2 CO 3 (पोटेशियम कार्बोनेट) का सूत्र इकाई द्रव्यमान = (2 x K का परमाणु द्रव्यमान) + (1 x C का परमाणु द्रव्यमान) + (3 x O का परमाणु द्रव्यमान) = (2 x 39 u) + (1 x 12 u) + (3 x 16 u) = 138 u
अतिरिक्त प्रश्न
अति लघु उत्तरीय प्रश्न
प्रश्न 1. द्रव्यमान संरक्षण के नियम को परिभाषित कीजिए।
उत्तर: रासायनिक अभिक्रिया में द्रव्यमान का न तो सृजन हो सकता है और न ही विनाश।
उदाहरण: 2Na + Cl 2 ——–> 2NaCl
2 x 23 + 2 x 35.5 ——> 2(23 + 35.5)
प्रश्न 2. स्थिर अनुपात के नियम की व्याख्या कीजिए।
उत्तर: किसी भी रासायनिक पदार्थ में तत्व हमेशा द्रव्यमान के अनुसार निश्चित अनुपात में उपस्थित होते हैं।
उदाहरण के लिए, जल में, हाइड्रोजन के द्रव्यमान और ऑक्सीजन के द्रव्यमान H : O का अनुपात हमेशा 1:8 होता है।
प्रश्न 3. परमाणु शब्द किसने गढ़ा?
उत्तर: जॉन डाल्टन ने परमाणु शब्द गढ़ा।
प्रश्न 4. परमाणु को परिभाषित कीजिए।
उत्तर: पदार्थ का सबसे छोटा कण, जो रासायनिक अभिक्रिया में भाग ले सकता है, परमाणु कहलाता है।
प्रश्न 5. अणु को परिभाषित कीजिए।
उत्तर: किसी तत्व या यौगिक का वह सबसे छोटा कण जो स्वतंत्र रूप से रह सकता है, अणु कहलाता है।
प्रश्न 6. परमाण्विकता को परिभाषित कीजिए।
उत्तर: किसी अणु में परमाणुओं की संख्या को उसकी परमाण्विकता कहते हैं।
प्रश्न 7. परमाणु द्रव्यमान इकाई क्या है?
उत्तर: किसी पदार्थ के अणु में उपस्थित सभी परमाणुओं के परमाणु द्रव्यमानों का योग परमाणु द्रव्यमान इकाई में व्यक्त किया जाता है। उदाहरण: H 2 0 = 1 x 2 + 16 = 18 amu
प्रश्न 8. परमाणु कैसे पाए जाते हैं?
उत्तर: परमाणु, अणु या आयन के रूप में पाए जाते हैं।
प्रश्न 9. फॉस्फोरस और नाइट्रोजन की परमाण्विकता बताइए।
उत्तर: फॉस्फोरस की परमाण्विकता P 4 अर्थात् 4 है
। नाइट्रोजन की परमाण्विकता N 2 अर्थात् 2 है।
प्रश्न 10. आयन क्या है?
उत्तर: आवेशित परमाणु को आयन कहते हैं। आयन धनात्मक आवेशित हो सकता है जिसे धनायन कहते हैं या ऋणात्मक आवेशित हो सकता है जिसे ऋणायन कहते हैं।
प्रश्न 11. धनायन और ऋणायन का एक उदाहरण दीजिए।
उत्तर: धनायन => Na +
ऋणायन => Cl –
प्रश्न 12. धनायन और ऋणायन में एक अंतर बताइए।
उत्तर: धनायन धनावेशित आयन होते हैं।
ऋणायन ऋणावेशित आयन होते हैं।
प्रश्न 13. अमोनियम सल्फेट का रासायनिक सूत्र बताइए।
उत्तर: अमोनियम सल्फेट
NH 4 + SO 4 2-
रासायनिक सूत्र —-> (NH 4 ) 2 S0 4 .
प्रश्न 14. आवोगाद्रो स्थिरांक क्या है?
उत्तर: आवोगाद्रो स्थिरांक (6.022 x 10 23 ) को कार्बन-12 के ठीक 12 ग्राम में मौजूद परमाणुओं की संख्या के रूप में परिभाषित किया जाता है।
प्रश्न 15. H 2 0 का आणविक द्रव्यमान ज्ञात कीजिए।
उत्तर: H 2 0 का आणविक द्रव्यमान
= (2 x 1) + (16)
= 2 + 16 = 18 u
लघु उत्तरीय प्रश्न
प्रश्न 1. परमाणु का आकार मापने की इकाई बताइए तथा हाइड्रोजन परमाणु का आकार बताइए।
उत्तर: परमाणु का आकार मापने की इकाई नैनोमीटर है, हाइड्रोजन परमाणु का आकार 10 -10 मीटर है।
प्रश्न 2. IUPAC क्या है, इसका एक कार्य बताइए?
उत्तर: IUPAC शुद्ध एवं अनुप्रयुक्त रसायन विज्ञान का अंतर्राष्ट्रीय संघ है। यह तत्वों के नामों को अनुमोदित करता है।
प्रश्न 3. सोडियम, पोटैशियम, सोना और पारे के लैटिन नाम बताइए।
उत्तर: सोडियम —> सोडियम, सोना —> ऑरम
पोटैशियम —> कैलियम, पारा —> हाइड्रैर्जिरम
प्रश्न 4. H 2 0, C0 2 तथा NH 3 में संयोजित तत्वों के द्रव्यमान का अनुपात क्या है ?
उत्तर: H 2 O संयोजित तत्वों के द्रव्यमान का अनुपात 2 : 16 —>1 : 8 (H : O)
C0 2 संयोजित तत्वों के द्रव्यमान का अनुपात 12 : 32 —>3 : 08 (C : O)
NH 3 संयोजित तत्वों के द्रव्यमान का अनुपात 14 : 3 —>14 : 3 (N : H)
प्रश्न 5. संयोजकता की परिभाषा दीजिए और निम्नलिखित तत्वों की संयोजकता बताइए:
मैग्नीशियम, एल्युमिनियम, क्लोरीन और कॉपर।
उत्तर: संयोजकता: किसी तत्व की संयोजन क्षमता को उसकी संयोजकता कहते हैं। निम्नलिखित तत्वों की संयोजकता:
मैग्नीशियम – 2
एल्युमिनियम – 3
क्लोरीन – 1
कॉपर – 2
प्रश्न 6. बहुपरमाणुक आयन क्या है? एक उदाहरण दीजिए।
उत्तर: आवेश धारण करने वाले परमाणुओं के समूह को बहुपरमाणुक आयन कहते हैं।
उदाहरण: अमोनियम – NH4 + नाइट्रेट
– N03 –
प्रश्न 7. कॉपर नाइट्रेट, कैल्शियम सल्फेट और एल्युमिनियम हाइड्रॉक्साइड का सूत्र लिखिए ।
उत्तर: रासायनिक सूत्र:
कॉपर नाइट्रेट —> Cu(N0 3 )
कैल्शियम सल्फेट —> CaS0 4 एल्युमिनियम हाइड्रॉक्साइड Al(OH) 3
प्रश्न 8. सूत्र इकाई द्रव्यमान क्या है? यह आण्विक द्रव्यमान से किस प्रकार भिन्न है?
उत्तर: किसी पदार्थ का सूत्र इकाई द्रव्यमान, यौगिक के सूत्र इकाई में उपस्थित सभी परमाणुओं के परमाणु द्रव्यमानों का योग होता है। सूत्र इकाई द्रव्यमान के अवयवी कण आयन होते हैं और आण्विक द्रव्यमान के अवयवी कण परमाणु होते हैं।
प्रश्न 9. निम्नलिखित में परमाणुओं की संख्या ज्ञात कीजिए:
(i) 0.5 मोल C परमाणु
(ii) 2 मोल N परमाणु
उत्तर: (i) 0.5 मोल C परमाणु:
1 मोल C परमाणु में परमाणुओं की संख्या = 6.022 x 10 23 परमाणु
0.5 मोल C परमाणु में परमाणुओं की संख्या = 6.022 x 10 23 x 0.5
= 3.011 x 10 23 परमाणु
(ii) 2 मोल N परमाणु:
1 मोल N परमाणु में परमाणुओं की संख्या = 6.022 x 10 23 परमाणु
2 मोल N परमाणु में परमाणुओं की संख्या = 6.022 x 2 x 10 23
= 1.2044 x 10 24 परमाणु
प्रश्न 10. निम्नलिखित का द्रव्यमान ज्ञात कीजिए:
(i) 6.022 x 10 23 O 2 अणुओं की संख्या
(ii) 1.5 मोल CO 2 अणु
उत्तर: (i) 6.022 x 10 23 O 2 अणुओं की संख्या:
1 मोल O 2 अणु का द्रव्यमान = 6.022 x 10 23 अणु = 32 ग्राम
(ii) 1.5 मोल CO 2 अणु: 1 मोल CO 2
अणु का द्रव्यमान = 6.022 x 10 23 अणु = 44 ग्राम 1.5 मोल C0 2 अणु का द्रव्यमान = 44 x 1.5 = 66 ग्राम
प्रश्न 11. किसी तत्व का प्रतीक लिखने के नियम क्या हैं?
उत्तर: IUPAC —> इंटरनेशनल यूनियन ऑफ प्योर एंड एप्लाइड केमिस्ट्री तत्वों के नामों को मंजूरी देता है।
प्रतीक अंग्रेजी में तत्व के नाम के पहले एक या दो अक्षर होते हैं। किसी प्रतीक का पहला अक्षर हमेशा बड़े अक्षर (अपर केस) और दूसरा अक्षर छोटे अक्षर (लोअर केस) के रूप में लिखा जाता है।
उदाहरण के लिए, हाइड्रोजन —> H हीलियम —> He
कुछ प्रतीक लैटिन, जर्मन या ग्रीक में तत्वों के नामों से लिए गए हैं।
उदाहरण के लिए, लोहे का प्रतीक Fe है, इसका लैटिन नाम फेरम है।
सोडियम का प्रतीक Na है, इसका लैटिन नाम नैट्रियम है।
प्रश्न 12. सापेक्ष परमाणु द्रव्यमान और सापेक्ष आणविक द्रव्यमान की व्याख्या कीजिए।
उत्तर: सापेक्ष परमाणु द्रव्यमान: इसे इस प्रकार परिभाषित किया जा सकता है कि किसी दिए गए तत्व का एक परमाणु कार्बन-12 के एक परमाणु के द्रव्यमान के 1/12वें भाग से कितनी बार भारी होता है। सापेक्ष आणविक द्रव्यमान: इसे इस प्रकार परिभाषित किया जाता है कि किसी पदार्थ या दिए गए तत्व का एक अणु कार्बन-12 के एक परमाणु के द्रव्यमान के 1/12वें भाग से कितनी बार भारी होता है।
प्रश्न 13. कार्बन डाइऑक्साइड का सूत्र CO2 है । इस सूत्र से आपको क्या जानकारी मिलती है?
उत्तर: (i) CO2 कार्बन डाइऑक्साइड को दर्शाता है।
(ii) CO2 कार्बन डाइऑक्साइड का एक अणु है।
(iii) CO2 कार्बन डाइऑक्साइड का एक मोल है, अर्थात इसमें कार्बन डाइऑक्साइड के 6.022 x 1023
अणु हैं। (iv) CO2 में कार्बन का 1 परमाणु और ऑक्सीजन के दो परमाणु हैं।
(v) CO2 44 ग्राम मोलर द्रव्यमान को दर्शाता है।
दीर्घ उत्तरीय प्रश्न
उत्तर: परमाणु बहुत छोटे होते हैं और उनके व्यक्तिगत द्रव्यमान की गणना नहीं की जा सकती क्योंकि यह नगण्य है। इसलिए परमाणुओं का द्रव्यमान एक निश्चित मानक के संबंध में इकाइयों में व्यक्त किया जाता है। शुरुआत में 1 द्रव्यमान वाले हाइड्रोजन परमाणु को डाल्टन ने मानक इकाई के रूप में लिया था। बाद में, इसे ऑक्सीजन परमाणु (0=16) से बदल दिया गया। लेकिन समस्थानिकों के कारण द्रव्यमान पूर्ण संख्या के बजाय अंशों में पाए गए। इसलिए, कार्बन (C=12) समस्थानिक को मानक इकाई के रूप में लिया गया और इसे सार्वभौमिक रूप से स्वीकार किया गया।
परमाणु द्रव्यमान इकाई कार्बन-12 के एक परमाणु के द्रव्यमान के बारहवें (1/12) के बराबर होती है, इसकी इकाई u है।
ग्राम परमाणु द्रव्यमान: जब किसी तत्व का परमाणु द्रव्यमान ग्राम में व्यक्त किया जाता है, तो उसे तत्व का ग्राम परमाणु द्रव्यमान कहा जाता है।
परमाणुओं, अणुओं का द्रव्यमान 'u' में व्यक्त किया जाता है और मोलों का द्रव्यमान यानी मोलर द्रव्यमान g में व्यक्त किया जाता है।
