NCERT Class 10 Science Chapter 3 धातु और अधातु
NCERT Solutions for Class 10 Science Chapter 3 धातु और अधातु
प्रश्न 1.
निम्नलिखित में से कौन सा युग्म विस्थापन अभिक्रिया देगा?
(a) NaCl विलयन और कॉपर धातु।
(b) MgCl विलयन और एल्युमीनियम धातु।
(c) FeSO विलयन और सिल्वर धातु।
(d) AgNO विलयन और कॉपर धातु।
उत्तर:
(d) AgNO विलयन और कॉपर धातु।
प्रश्न 2.
लोहे के तवे को जंग लगने से बचाने के लिए निम्नलिखित में से कौन सी विधि उपयुक्त है?
(a) ग्रीस लगाना
(b) पेंट लगाना
(c) जिंक की परत लगाना
(d) उपरोक्त सभी
उत्तर:
(c) जिंक की परत लगाना
प्रश्न 3.
एक तत्व ऑक्सीजन के साथ अभिक्रिया करके उच्च गलनांक वाला यौगिक देता है। यह यौगिक जल में भी घुलनशील है। यह तत्व संभवतः
(a) कैल्शियम
(b) कार्बन
(c) सिलिकॉन
(d) लोहा है।
उत्तर:
(a) कैल्शियम।
प्रश्न 4.
खाद्य डिब्बों पर टिन की परत चढ़ाई जाती है, जिंक की नहीं, क्योंकि
(a) जिंक टिन से महंगा है।
(b) जिंक का गलनांक टिन से अधिक है।
(c) जिंक टिन से कम क्रियाशील है।
(d) जिंक टिन से अधिक क्रियाशील है।
उत्तर:
(d) जिंक टिन से अधिक क्रियाशील है।
प्रश्न 5.
आपको एक हथौड़ा, एक बैटरी, एक बल्ब, तार और एक स्विच दिया गया है।
(a) आप इनका उपयोग धातुओं और अधातुओं के नमूनों में अंतर करने के लिए कैसे कर सकते हैं?
(b) धातुओं और अधातुओं के बीच अंतर करने में इन परीक्षणों की उपयोगिता का आकलन कीजिए।
उत्तर:
(a) धातुओं को बिना तोड़े हथौड़े से पीटकर पतली चादरें बनाई जा सकती हैं। अधातुओं को हथौड़े से पीटकर पतली चादरें नहीं बनाई जा सकतीं। हथौड़े से मारने पर अधातु टुकड़ों में टूट जाती हैं। धातुएँ आघातवर्ध्य होती हैं, जबकि अधातुएँ अगलने योग्य होती हैं। जब धातुओं को बैटरी, बल्ब, तारों और स्विच का उपयोग करके परिपथ में जोड़ा जाता है, तो परिपथ से धारा प्रवाहित होती है और बल्ब चमक उठता है। जब अधातुएँ (जैसे सल्फर) जुड़ी होती हैं, तो बल्ब बिल्कुल भी नहीं जलता है। धातुएँ विद्युत की अच्छी सुचालक होती हैं।
(b) आघातवर्ध्यता के कारण, धातुओं को चादरों के रूप में ढाला जा सकता है। धातुएँ विद्युत की अच्छी सुचालक होती हैं इसलिए इनका उपयोग विद्युत केबलों के लिए किया जा सकता है।
प्रश्न 6.
उभयधर्मी ऑक्साइड क्या हैं? उभयधर्मी ऑक्साइड के दो उदाहरण दीजिए।
अथवा
रासायनिक समीकरण लिखिए जो दर्शाते हैं कि एल्युमिनियम ऑक्साइड अम्ल और क्षार दोनों के साथ अभिक्रिया करता है। [CBSE2011]
उत्तर:
वे धातु ऑक्साइड जो क्षारीय और अम्लीय दोनों व्यवहार प्रदर्शित करते हैं, उभयधर्मी ऑक्साइड कहलाते हैं। दूसरे शब्दों में, वे धातु ऑक्साइड जो अम्ल और क्षार दोनों के साथ अभिक्रिया करके लवण और जल बनाते हैं, उभयधर्मी ऑक्साइड कहलाते हैं। एल्युमिनियम ऑक्साइड और जिंक ऑक्साइड उभयधर्मी प्रकृति के होते हैं।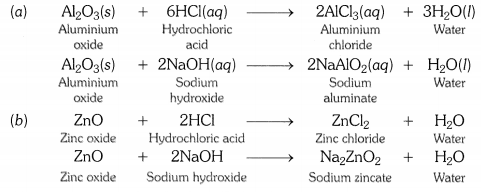
प्रश्न 7.
दो धातुओं के नाम बताइए जो तनु अम्लों से हाइड्रोजन को विस्थापित कर देंगी और दो धातुओं के नाम बताइए जो ऐसा नहीं करेंगी।
उत्तर:
(i) क्रियाशीलता श्रेणी में हाइड्रोजन से ऊपर की धातुएँ, जैसे सोडियम और मैग्नीशियम, तनु अम्लों से हाइड्रोजन को विस्थापित करती हैं।
(ii) क्रियाशीलता श्रेणी में हाइड्रोजन से नीचे की धातुएँ, जैसे कॉपर, सिल्वर, तनु अम्लों से हाइड्रोजन को विस्थापित नहीं करती हैं।
प्रश्न 8.
किसी धातु M के विद्युत अपघटनी शोधन में, आप एनोड, कैथोड और विद्युत अपघट्य के रूप में क्या लेंगे?
उत्तर:
कैथोड – शुद्ध धातु
एनोड – अशुद्ध धातु
विद्युत अपघट्य – धातु लवण विलयन
प्रश्न 9.
प्रत्यूष ने सल्फर पाउडर को एक स्पैचुला पर लिया और उसे गर्म किया। उसने एक परखनली को उसके ऊपर उलटकर, उससे निकली गैस को एकत्र किया, जैसा कि चित्र में दिखाया गया है। (a) गैस की (i) शुष्क लिटमस पत्र
पर क्या क्रिया होगी ? (ii) आर्द्र लिटमस पत्र पर क्या क्रिया होगी? (b) होने वाली अभिक्रिया के लिए एक संतुलित रासायनिक समीकरण लिखिए। उत्तर: (i) शुष्क लिटमस पत्र - कोई क्रिया नहीं। (ii) आर्द्र लिटमस पत्र - लाल हो जाता है।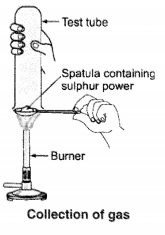
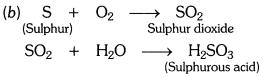
प्रश्न 10.
लोहे को जंग लगने से बचाने के दो तरीके बताइए।
उत्तर:
लोहे को जंग लगने से बचाने के तरीके हैं:
(a) पेंटिंग द्वारा
(b) गैल्वनाइजिंग द्वारा
प्रश्न 11.
अधातुएँ ऑक्सीजन के साथ संयोग करके किस प्रकार के ऑक्साइड बनाती हैं?
उत्तर:
अधातुएँ ऑक्सीजन के साथ संयोग करके अम्लीय ऑक्साइड या उदासीन ऑक्साइड बनाती हैं।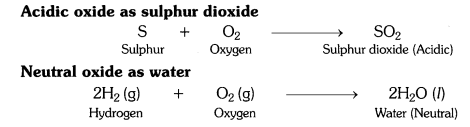
प्रश्न 12.
कारण बताइए :
(a) प्लैटिनम, सोना और चांदी का उपयोग आभूषण बनाने के लिए किया जाता है।
(b) सोडियम, पोटेशियम और लिथियम को तेल के नीचे रखा जाता है।
(c) एल्युमिनियम एक अत्यधिक प्रतिक्रियाशील धातु है, फिर भी इसका उपयोग खाना पकाने के बर्तन बनाने के लिए किया जाता है।
(d) कार्बोनेट और सल्फाइड अयस्क आमतौर पर निष्कर्षण की प्रक्रिया के दौरान ऑक्साइड में परिवर्तित हो जाते हैं।
उत्तर:
(a) प्लैटिनम, सोना और चांदी का उपयोग आभूषण बनाने के लिए किया जाता है क्योंकि ये आघातवर्धनीय और तन्य होते हैं। ये संक्षारण के प्रति अत्यधिक प्रतिरोधी होते हैं।
(b) सोडियम, पोटेशियम और लिथियम बहुत प्रतिक्रियाशील होते हैं और हवा के संपर्क में आने पर आग पकड़ लेते हैं। ऐसा उनके कम ज्वलन तापमान और उच्च प्रतिक्रियाशीलता के कारण होता है।
(c) एल्युमिनियम अपनी सतह पर एल्युमिनियम ऑक्साइड की एक गैर-प्रतिक्रियाशील परत बनाता है। यह परत एल्युमिनियम को अन्य पदार्थों के साथ प्रतिक्रिया करने से रोकती है। इसलिए एल्युमिनियम का उपयोग खाना पकाने के बर्तन बनाने के लिए किया जाता है।
(d) किसी धातु ऑक्साइड को मुक्त धातु में कम करना आसान होता है। चूंकि धातुओं को उनके कार्बोनेट या सल्फाइड से सीधे प्राप्त करने की तुलना में उनके ऑक्साइड से प्राप्त करना आसान होता है, इसलिए धातुओं को निकालने के लिए कार्बोनेट और सल्फाइड अयस्कों को पहले ऑक्साइड में परिवर्तित किया जाता है।
प्रश्न 13.
आपने तांबे के बर्तनों को नींबू या इमली के रस से साफ़ होते देखा होगा। बताइए कि ये खट्टे पदार्थ बर्तनों को साफ़ करने में प्रभावी क्यों होते हैं।
उत्तर:
नींबू या इमली के रस जैसे खट्टे पदार्थों में अम्ल होते हैं। ये अम्ल तांबे के बर्तनों की सतह पर मौजूद कॉपर ऑक्साइड या बेसिक कॉपर कार्बोनेट की परत को घोलकर उन्हें फिर से चमकदार लाल-भूरा बना देते हैं।
प्रश्न 14.
एक आदमी सुनार बनकर घर-घर गया। उसने पुराने और फीके सोने के गहनों की चमक वापस लाने का वादा किया। एक अनजान महिला ने उसे सोने की चूड़ियों का एक सेट दिया, जिसे उसने एक खास घोल में डुबोया। चूड़ियाँ नई जैसी चमक उठीं, लेकिन उनका वजन काफी कम हो गया। महिला परेशान हुई, लेकिन व्यर्थ की बहस के बाद उस आदमी ने जल्दबाजी में दोहराया। क्या आप जासूस बनकर उसके द्वारा इस्तेमाल किए गए घोल की प्रकृति का पता लगा सकते हैं?
उत्तर:
बेईमान सुनार ने सोने की चूड़ियों को एक्वा-रेजिया (जिसमें आयतन के हिसाब से 1 भाग सांद्र नाइट्रिक अम्ल और 3 भाग सांद्र हाइड्रोक्लोरिक अम्ल होता है) में डुबोया। एक्वा-रेजिया ने सोने की चूड़ियों से काफी मात्रा में सोना घोल दिया और इस तरह उनका वजन काफी कम हो गया। बेईमान सुनार एक उपयुक्त उपचार द्वारा एक्वा-रेजिया से घुले हुए सोने को पुनः प्राप्त कर सकता है।
एनसीईआरटी समाधान
धातु और अधातु: धातुओं और अधातुओं के गुण, प्रतिक्रियाशीलता श्रृंखला, आयनिक यौगिकों का निर्माण और गुण, मूल धातुकर्म प्रक्रियाएं, संक्षारण और इसकी रोकथाम।
प्रश्न 1
उभयधर्मी ऑक्साइड क्या हैं? उभयधर्मी ऑक्साइड के दो उदाहरण दीजिए।
उत्तर:
उभयधर्मी ऑक्साइड वे ऑक्साइड होते हैं जो अम्ल और क्षार दोनों के साथ अभिक्रिया करके लवण और जल बनाते हैं। उदाहरण: ZnO और Al 2 O 3 ।
प्रश्न 2
दो धातुओं के नाम बताइए जो तनु अम्लों से हाइड्रोजन को विस्थापित कर सकती हैं, और दो धातुओं के नाम बताइए जो ऐसा नहीं कर सकतीं।
हल:
Zn और Mg जैसी अति अभिक्रियाशील धातुएँ तनु अम्लों से हाइड्रोजन को विस्थापित करती हैं। दूसरी ओर, Cu, Ag आदि जैसी कम अभिक्रियाशील धातुएँ तनु अम्लों से हाइड्रोजन को विस्थापित नहीं करतीं।
प्रश्न 3
किसी धातु M के विद्युत अपघटनी शोधन में, आप एनोड, कैथोड और विद्युत अपघट्य के रूप में क्या लेंगे?
हल:
एनोड धातु M का अशुद्ध, मोटा ब्लॉक है।
कैथोड शुद्ध धातु M की एक पतली पट्टी/तार है।
विद्युत अपघट्य धातु M का एक उपयुक्त लवण विलयन है।
प्रश्न 4
लोहे को जंग लगने से बचाने के दो उपाय बताइए।
समाधान:
लोहे की सतह पर जंगरोधी पेंट लगाकर।
लोहे की वस्तुओं की सतह पर तेल या ग्रीस लगाकर, जिससे नमी युक्त हवा की आपूर्ति सतह से बंद हो जाए।
प्रश्न 5
जब अधातुएँ ऑक्सीजन के साथ संयोग करती हैं तो किस प्रकार के ऑक्साइड बनते हैं?
उत्तर:
जब अधातुएँ ऑक्सीजन के साथ संयोग करती हैं तो वे या तो उदासीन या अम्लीय ऑक्साइड बनाती हैं। CO एक उदासीन ऑक्साइड है; N 2 O 5 या N 2 O 3 एक अम्लीय ऑक्साइड है।
प्रश्न 6
कारण बताइए
i. धातुएँ तनु अम्लों से हाइड्रोजन का स्थान लेती हैं, जबकि अधातुएँ ऐसा नहीं करती हैं।
ii. निष्कर्षण की प्रक्रिया के दौरान कार्बोनेट और सल्फाइड अयस्क आमतौर पर ऑक्साइड में परिवर्तित हो जाते हैं।
हल:
i. धातुएँ प्रकृति में विद्युत धनात्मक होती हैं। वे आसानी से इलेक्ट्रॉन खो देते हैं। ये इलेक्ट्रॉन अम्ल से मुक्त प्रोटॉन को कम करके हाइड्रोजन गैस मुक्त करते हैं, जबकि अधातुओं में इलेक्ट्रॉन ग्रहण करने की प्रवृत्ति होती है और इसलिए वे अम्लों से मुक्त प्रोटॉन को इलेक्ट्रॉन प्रदान नहीं करते हैं। इसलिए H2 गैस मुक्त नहीं होती है।
ii. चूँकि धातु ऑक्साइड को धातु में कम करना आसान होता है, इसलिए अपचयन से पहले, धातु सल्फाइड और कार्बोनेट को ऑक्साइड में बदलना चाहिए।
प्रश्न 7
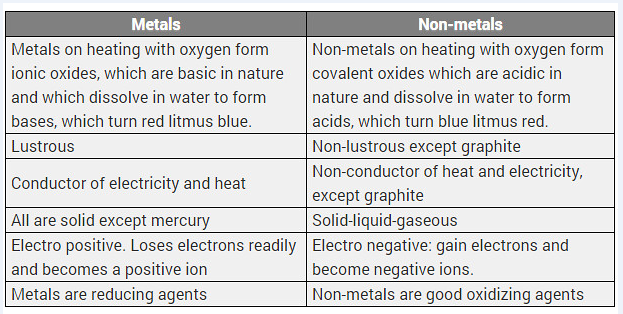
धातुओं और अधातुओं में उनके रासायनिक गुणों के आधार पर अंतर बताइए
।
प्रश्न 8
समझाइए कि कुछ धातुओं की सतह लंबे समय तक हवा के संपर्क में रहने पर फीकी क्यों पड़ जाती है।
उत्तर:
ऐसा नम हवा के संपर्क में आने पर धातुओं के सतही ऑक्सीकरण के कारण होता है। उदाहरण के लिए, कॉपर की सतह क्षारीय कॉपर कार्बोनेट Cu(OH) 2 · CuCO 3 के बनने के कारण हरी हो जाती है। इसी प्रकार, चांदी काले Ag 2 S के बनने के कारण काली हो जाती है और एल्युमीनियम की सतह पर Al2O3 की एक सफेद परत बन जाती है।
प्रश्न 9
बताइए कि निम्नलिखित में से कौन सी धातु तनु हाइड्रोक्लोरिक अम्ल में मिलाने पर हाइड्रोजन देगी: i. लोहा, ii. तांबा, iii. मैग्नीशियम।
तांबा तनु हाइड्रोक्लोरिक अम्ल के साथ बिल्कुल भी अभिक्रिया नहीं करता है। इससे पता चलता है कि तांबा, लोहे से भी कम अभिक्रियाशील है।
प्रश्न 10
एक अधात्विक तत्व का नाम बताइए जो विद्युत का संचालन करता है।
हल:
ग्रेफाइट के रूप में कार्बन विद्युत का संचालन करता है, क्योंकि प्रत्येक कार्बन परमाणु में एक मुक्त इलेक्ट्रॉन होता है, जो षट्कोणीय परतों के बीच स्वतंत्र रूप से घूमता है।
प्रश्न 11
कौन सी धातुएँ आसानी से संक्षारित नहीं होतीं?
उत्तर:
सोना, प्लैटिनम और अन्य उत्कृष्ट धातुएँ हवा में संक्षारित नहीं होतीं।
प्रश्न 12
मिश्र धातुएँ क्या हैं?
उत्तर:
मिश्र धातुएँ दो या दो से अधिक धातुओं, या एक धातु और एक अधातु का समांगी मिश्रण होती हैं। जैसे: स्टील, पीतल, कांसा, आदि।
प्रश्न 13
निम्नलिखित शब्दों को परिभाषित करें।
(i) खनिज
(ii) अयस्क
(iii) गैंग
हल:
(i) खनिज
सभी यौगिक या तत्व, जो पृथ्वी की पपड़ी में प्राकृतिक रूप से पाए जाते हैं, खनिज कहलाते हैं। उदाहरण: फिटकरी, K 2 SO 4 .Al 2 (SO 4 ) 3 .24 H 2 O, बॉक्साइट Al 2 O 3 .2H 2 O
(ii) अयस्क
वे खनिज जिनसे किसी धातु को लाभप्रद रूप से निकाला जा सकता है, अयस्क कहलाते हैं। बॉक्साइट (Al 2 O 3 .2H 2 O) Al, कॉपर पाइराइट CuFeS 2 का अयस्क है । सभी खनिज अयस्क नहीं हैं लेकिन सभी अयस्क खनिज हैं।
(iii) गैंग
जब किसी अयस्क को पृथ्वी से खनन किया जाता है, तो यह हमेशा रेत चट्टानी पदार्थों से दूषित पाया जाता है। अयस्क में मौजूद रेत और चट्टान सामग्री की अशुद्धता को गैंग के रूप में जाना जाता है।
प्रश्न 14
प्रकृति में मुक्त अवस्था में पाई जाने वाली दो धातुओं के नाम लिखिए।
उत्तर:
सोना और प्लैटिनम प्रकृति में मुक्त अवस्था में पाए जाते हैं।
प्रश्न 15
किसी धातु को उसके ऑक्साइड से प्राप्त करने के लिए प्रयुक्त रासायनिक प्रक्रिया क्या है?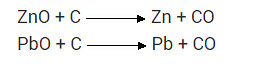
प्रश्न 16
दो धातुओं के नाम बताइए, जो धातुओं के साथ हाइड्राइड बना सकती हैं।
हल:
सोडियम और कैल्शियम हाइड्रोजन के साथ अभिक्रिया करके स्थायी हाइड्राइड बनाते हैं।
प्रश्न 17
क्या प्रत्येक खनिज का एक निश्चित और स्थिर संघटन होता है? व्याख्या कीजिए।
उत्तर:
हाँ, प्रत्येक खनिज का एक निश्चित और स्थिर संघटन होता है। खनिज पृथ्वी की पपड़ी में ऑक्साइड, कार्बोनेट, सल्फाइड, सल्फेट, नाइट्रेट आदि के रूप में व्यापक रूप से वितरित हैं। ये खनिज पृथ्वी के निर्माण के दौरान होने वाले रासायनिक परिवर्तनों के परिणामस्वरूप बने हैं।
प्रश्न 18
आघातवर्धनीय और तन्य का अर्थ स्पष्ट कीजिए।
हल:
आघातवर्धनीय वह है जिसे पीटकर/हथौड़े से पीटकर पतली चादरें बनाई जा सकती हैं।
तन्य वह है जिसे खींचकर पतले तार बनाए जा सकते हैं।
प्रश्न 19
i. सोडियम, ऑक्सीजन और मैग्नीशियम की इलेक्ट्रॉन बिंदु संरचनाएँ लिखिए। ii. इलेक्ट्रॉन स्थानांतरण द्वारा MgO और Na2O का निर्माण दर्शाइए। iii
. इन यौगिकों में कौन-से आयन उपस्थित हैं? हल: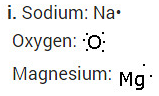
ii. मैग्नीशियम ऑक्साइड का निर्माण
जब मैग्नीशियम ऑक्सीजन के साथ अभिक्रिया करता है, तो मैग्नीशियम परमाणु अपने दो सबसे बाहरी इलेक्ट्रॉनों को एक ऑक्सीजन परमाणु में स्थानांतरित कर देता है। 2 इलेक्ट्रॉन खोकर, मैग्नीशियम परमाणु एक मैग्नीशियम आयन (Mg 2+ ) बनाता है और 2 इलेक्ट्रॉन प्राप्त करके, ऑक्सीजन परमाणु एक ऑक्साइड आयन (O 2- ) बनाता है।![]()
सोडियम ऑक्साइड का निर्माण
दो सोडियम परमाणु अपने दो सबसे बाहरी इलेक्ट्रॉन एक ऑक्सीजन परमाणु को स्थानांतरित करते हैं। दो इलेक्ट्रॉन खोकर, दो सोडियम परमाणु दो सोडियम आयन (2Na + ) बनाते हैं। और दो इलेक्ट्रॉन प्राप्त करके, ऑक्सीजन परमाणु एक ऑक्साइड आयन (O 2- ) बनाता है।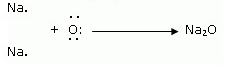
iii. सोडियम ऑक्साइड यौगिक (Na 2 0) में मौजूद आयन सोडियम आयन (2Na +) और ऑक्साइड आयन (O 2- ) हैं।
मैग्नीशियम ऑक्साइड यौगिक (MgO) में मौजूद आयन मैग्नीशियम आयन Mg 2+ और ऑक्साइड आयन (O 2- ) हैं।
प्रश्न 20
आपने तांबे के बर्तनों को नींबू या इमली के रस से साफ होते देखा होगा। समझाइए कि ये खट्टे पदार्थ बर्तनों की सफाई में प्रभावी क्यों होते हैं।
हल:
नींबू (या इमली के रस) जैसे खट्टे पदार्थों में अम्ल होते हैं। ये अम्ल तांबे के बर्तनों की सतह पर मौजूद कॉपर ऑक्साइड या बेसिक कॉपर कार्बोनेट की परत को घोलकर उन्हें फिर से चमकदार लाल-भूरा बना देते हैं।
प्रश्न 21
एक ऐसी धातु का उदाहरण दीजिए जो
i. कमरे के तापमान पर द्रव अवस्था में होती है।
ii. चाकू से आसानी से काटी जा सकती है।
iii. ऊष्मा की सबसे अच्छी चालक होती है।
iv. ऊष्मा की कुचालक होती है।
हल:
i. पारा कमरे के तापमान पर द्रव अवस्था में होता है।
ii. सोडियम और पोटेशियम नरम धातुएँ हैं जिन्हें चाकू से आसानी से काटा जा सकता है।
iii. चाँदी विद्युत की सबसे अच्छी चालक होती है।
iv. पारा ऊष्मा का कुचालक होता है।
प्रश्न 22
सोडियम को मिट्टी के तेल में क्यों डुबोकर रखा जाता है?
उत्तर:
सोडियम धातु को हवा की ऑक्सीजन, नमी और कार्बन डाइऑक्साइड के साथ प्रतिक्रिया से बचाने के लिए मिट्टी के तेल में डुबोकर रखा जाता है।
प्रश्न 23
आयनिक यौगिकों के गलनांक उच्च क्यों होते हैं?
उत्तर:
ये यौगिक धनात्मक और ऋणात्मक आयनों से बने होते हैं। विपरीत आवेशित आयनों के बीच प्रबल आकर्षण बल होता है, इसलिए इस आकर्षण बल को तोड़ने और आयनिक यौगिकों को पिघलाने के लिए अत्यधिक ऊष्मा ऊर्जा की आवश्यकता होती है। यही कारण है कि आयनिक यौगिकों के गलनांक उच्च होते हैं।
प्रश्न 24
एक आदमी सुनार बनकर घर-घर गया। उसने पुराने और फीके सोने के गहनों की चमक वापस लाने का वादा किया। एक अनजान महिला ने उसे सोने की चूड़ियों का एक सेट दिया, जिसे उसने एक खास घोल में डुबोया। चूड़ियाँ बिल्कुल नई जैसी चमक उठीं, लेकिन उनका वज़न बहुत कम हो गया। महिला परेशान हुई, लेकिन व्यर्थ की बहस के बाद वह आदमी जल्दी से वहाँ से चला गया। क्या आप जासूस बनकर उस घोल की प्रकृति का पता लगा सकते हैं जो उसने इस्तेमाल किया था?
घोल:
एक्वा रेजिया (आयतन के अनुसार, इसमें 3 भाग सांद्र हाइड्रोक्लोरिक अम्ल और 1 भाग सांद्र नाइट्रिक अम्ल होता है) वह घोल है, जिसका उपयोग चूड़ियों को नई जैसी चमक देने के लिए किया जाता है, लेकिन इससे उनका वज़न बहुत कम हो जाता है।
प्रश्न 25 (i) लोहे के साथ जल (ii) कैल्शियम और पोटेशियम के साथ जल
की अभिक्रियाओं के लिए समीकरण लिखिए ।
हल:
प्रश्न 26
जब जिंक को सोडियम या आयरन (II) सल्फेट में मिलाया जाता है, तो आप क्या देखते हैं? होने वाली रासायनिक अभिक्रिया लिखिए।
हल:
जिंक, आयरन की तुलना में अधिक अभिक्रियाशील (अधिक विद्युत धनात्मक) होता है। इसलिए यह आयरन को उसके लवण विलयन से विस्थापित कर देता है। फेरस सल्फेट का रंग हल्का हरा होता है, जो रंगहीन हो जाता है।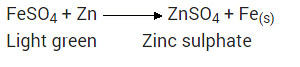
प्रश्न 27
प्रत्यूष ने सल्फर पाउडर को एक स्पैचुला पर लिया और उसे गर्म किया। उसने जलते हुए सल्फर के ऊपर एक परखनली उलटकर उससे निकली गैस एकत्र की।
इस गैस की क्रिया क्या होगी:
सूखे लिटमस पत्र पर?
नम लिटमस पत्र पर?
होने वाली अभिक्रिया के लिए एक संतुलित रासायनिक समीकरण लिखिए।
हल:
a) जब सल्फर को हवा में जलाया जाता है तो सल्फर डाइऑक्साइड गैस बनती है।
(i) सल्फर डाइऑक्साइड गैस की सूखे लिटमस पत्र पर कोई क्रिया नहीं होती।
(ii) सल्फर डाइऑक्साइड गैस नम नीले लिटमस पत्र को लाल कर देती है।
(b) S (s) + O 2(g) —> SO 2(g)
